| –Т–Є–і—Л –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л—Е –љ–∞–љ–Њ—Б—В—А—Г–Ї—В—Г—А | |
| –≠–љ—Ж–Є–Ї–ї–Њ–њ–µ–і–Є—П - –Т–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Є —А–∞–Ј–≤–Є—В–Є–µ –љ–∞–љ–Њ–љ–∞—Г–Ї–Є |
|
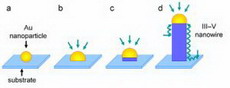
–°–∞–Љ—Л–µ —Г–і–Є–≤–Є—В–µ–ї—М–љ—Л–µ –Є –њ–Њ–ї–µ–Ј–љ—Л–µ –Є–Ј–Њ–±—А–µ—В–µ–љ–Є—П –љ–µ –њ—А–Є–љ–∞–і–ї–µ–ґ–∞—В –Ї —З–Є—Б–ї—Г —В–µ—Е, –Ї–Њ—В–Њ—А—Л–µ –і–µ–ї–∞—О—В –Љ–љ–Њ–≥–Њ —З–µ—Б—В–Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–Љ—Г —Г–Љ—Г. –°–∞–Љ—Л–Љ –њ—А–Њ—Б—В—Л–Љ –љ–∞–љ–Њ–Љ–∞—В–µ—А–Є–∞–ї–Њ–Љ –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М —Д—А–∞–≥–Љ–µ–љ—В—Л –≤–µ—Й–µ—Б—В–≤–∞, –Є–Ј–Љ–µ–ї—М—З–µ–љ–љ—Л–µ –і–Њ –љ–∞–љ–Њ—А–∞–Ј–Љ–µ—А–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є–ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –Ї–∞–Ї–Є–Љ-—В–Њ –і—А—Г–≥–Є–Љ —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ –Є–ї–Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ. –•–Њ—В—П –±—Л –≤ –Њ–і–љ–Њ–Љ –Є–Ј–Љ–µ—А–µ–љ–Є–Є –Њ–љ–Є –і–Њ–ї–ґ–љ—Л –Є–Љ–µ—В—М –њ—А–Њ—В—П–ґ–µ–љ–љ–Њ—Б—В—М –љ–µ –±–Њ–ї–µ–µ 100 –љ–Љ –Є –њ—А–Њ—П–≤–ї—П—В—М –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ –љ–Њ–≤—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ (—Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ, —Н–Ї—Б–њ–ї—Г–∞—В–∞—Ж–Є–Њ–љ–љ—Л–µ –Є –і—А.) –†–µ–∞–ї—М–љ–Њ –і–Є–∞–њ–∞–Ј–Њ–љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ—Л—Е –Њ–±—К–µ–Ї—В–Њ–≤ –≥–Њ—А–∞–Ј–і–Њ —И–Є—А–µ вАФ –Њ—В –Њ—В–і–µ–ї—М–љ—Л—Е –∞—В–Њ–Љ–Њ–≤ (—А–∞–Ј–Љ–µ—А–Њ–Љ –Љ–µ–љ–µ–µ 0,1 –љ–Љ) –і–Њ –Є—Е –Ї–Њ–љ–≥–ї–Њ–Љ–µ—А–∞—В–Њ–≤ –Є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —Б–≤—Л—И–µ –Ѓ9 –∞—В–Њ–Љ–Њ–≤ –Є –Є–Љ–µ—О—Й–Є—Е —А–∞–Ј–Љ–µ—А—Л –і–∞–ґ–µ –±–Њ–ї–µ–µ 1 –Љ–Ї–Љ –≤ –Њ–і–љ–Њ–Љ –Є–ї–Є –і–≤—Г—Е –Є–Ј–Љ–µ—А–µ–љ–Є—П—Е. –Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –≤–∞–ґ–љ–Њ, —З—В–Њ –Њ–љ–Є —Б–Њ—Б—В–Њ—П—В –Є–Ј –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —З–Є—Б–ї–∞ –∞—В–Њ–Љ–Њ–≤, –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –≤ –љ–Є—Е —Г–ґ–µ –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –і–Є—Б–Ї—А–µ—В–љ–∞—П –∞—В–Њ–Љ–љ–Њ-–Љ–Њ-–ї–µ–Ї—Г–ї—П—А–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –≤–µ—Й–µ—Б—В–≤–∞, –Ї–≤–∞–љ—В–Њ–≤—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є —Н–љ–µ—А–≥–µ—В–Є–Ї–∞ —А–∞–Ј–≤–Є—В–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –љ–∞–љ–Њ—Б—В—А—Г–Ї—В—Г—А. –Э–∞–љ–Њ—Б—В—А—Г–Ї—В—Г—А—Л –Њ–±–ї–∞–і–∞—О—В —Б–Њ—З–µ—В–∞–љ–Є–µ–Љ —А—П–і–∞ –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —П–≤–ї–µ–љ–Є–є, –љ–µ—Б–≤–Њ–є—Б—В–≤–µ–љ–љ—Л—Е —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ –Љ–Њ–љ–Њ-–Ш –њ–Њ–ї–Є–Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤. –£–Љ–µ–љ—М—И–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–∞ –Ї—А–Є—Б—В–∞–ї–ї–Њ–≤ (–≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М вАФ –≤ –Љ–µ—В–∞–ї–ї–∞—Е –Є —Б–њ–ї–∞–≤–∞—Е) –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–≤–Њ–є—Б—В–≤ –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Н—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ—П–≤–ї—П—О—В—Б—П, –Ї–Њ–≥–і–∞ —Б—А–µ–і–љ–Є–є —А–∞–Ј–Љ–µ—А –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є—Е –Ј–µ—А–µ–љ –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 100 –љ–Љ, –∞ –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –њ—А–Є —А–∞–Ј–Љ–µ—А–µ –Ј–µ—А–µ–љ –Љ–µ–љ–µ–µ 10 –љ–Љ. –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В–Є—Ж—Л –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М —Б—Д–µ—А–Є—З–µ—Б–Ї—Г—О (—А–∞–≤–љ–Њ—А–∞–Ј–Љ–µ—А–љ—Г—О) —Д–Њ—А–Љ—Г, –±—Л—В—М –≤—Л—В—П–љ—Г—В—Л–Љ–Є –≤ –≤–Є–і–µ –љ–∞-–љ–Њ–њ—А–Њ–≤–Њ–ї–Њ–Ї–Є –Є–ї–Є –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞ –Є–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—В—М —Б–Њ–±–Њ–є –љ–∞-–љ–Њ—З–µ—И—Г–є–Ї–Є (–њ–ї–∞—Б—В–Є–љ–Ї–Є). –У–ї–∞–≤–љ–Њ–µ, —З—В–Њ–±—Л –Њ–і–љ–Њ –Є–Ј –Є–Ј–Љ–µ—А–µ–љ–Є–є (–і–Є–∞–Љ–µ—В—А —И–∞—А–Є–Ї–Њ–≤ –Є–ї–Є —В–Њ–ї—Й–Є–љ–∞ —З–µ—И—Г–µ–Ї) –љ–µ –њ—А–µ–≤—Л—И–∞–ї–Њ 100 –љ–Љ. –Э–∞ —А–Є—Б. 10 –њ–Њ–Ї–∞–Ј–∞–љ—Л —Б—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –љ–∞–љ–Њ—А–∞–Ј–Љ–µ—А–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –Ї—А–µ–Љ–љ–Є—П, –Ј–і–µ—Б—М –і–Є–∞–Љ–µ—В—А 84% —З–∞—Б—В–Є—Ж вАФ 44 –љ–Љ, –∞ 16% вАФ 14 –љ–Љ. –≠—В–Њ—В –љ–∞–љ–Њ—А–∞–Ј–Љ–µ—А–љ—Л–є –Ї—А–µ–Љ–љ–Є–є –њ–Њ–ї—Г—З–µ–љ –њ—А–Є —А–∞–Ј–ї–Њ–ґ–µ–љ–Є–Є –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–љ–Њ–≥–Њ –Љ–Њ–љ–Њ—Б–Є–ї–∞–љ–∞ (–Ї—А–µ–Љ–љ–µ–≤–Њ–і–Њ—А–Њ–і–∞) SiH4, –Є–Ј –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ–Њ–ї—Г—З–∞—О—В —З–Є—Б—В—Л–є –њ–Њ–ї—Г–њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤—Л–є –Ї—А–µ–Љ–љ–Є–є –≤ –Є–љ–µ—А—В–љ–Њ–є —Б—А–µ–і–µ –њ—А–Є —А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–Љ –њ–Њ–≥–ї–Њ—Й–µ–љ–Є–Є –ї–∞–Ј–µ—А–љ–Њ–≥–Њ –Є–Ј–ї—Г—З–µ–љ–Є—П. –Э–∞ —А–Є—Б. 11 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞ –њ–Њ–ї–Є—В–µ—В—А–∞—Д—В–Њ—А—Н—В–Є–ї–µ–љ–∞ (–Я–Ґ–§–≠), –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ–Њ —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ-–ї—Г—З–µ–≤–Њ–є —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ —Г–ї—М—В—А–∞–і–Є—Б–њ–µ—А—Б–љ–Њ–≥–Њ –Я–Ґ–§–≠. –Ф–Є–∞–Љ–µ—В—А –љ–∞-–љ–Њ–≤–Њ–ї–Њ–Ї–Њ–љ вАФ 40вАФ60 –љ–Љ –њ—А–Є –і–ї–Є–љ–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–Є–Ї—А–Њ–Љ–µ—В—А–Њ–≤. –Т –У–Њ—А–Њ–і—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ –У–Њ–љ–Ї–Њ–љ–≥–∞ –≥—А—Г–њ–њ–∞ —Г—З–µ–љ—Л—Е –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –®–Є—В-–Ґ—Г–љ–≥ –Ы–Є ( Suit - Tong Lee) —Б–Њ–Ј–і–∞–ї–∞ —Б–∞–Љ–Њ–µ –Љ–Є–љ–Є–∞—В—О—А–љ–Њ–µ –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–Њ –≤ –Љ–Є—А–µ (–µ–≥–Њ –і–Є–∞–Љ–µ—В—А —А–∞–≤–µ–љ 1,3 –љ–Љ), –Є—Б–њ–Њ–ї—М–Ј—Г—П –Љ–µ—В–Њ–і–Є–Ї—Г –≤—Л—А–∞—Й–Є–≤–∞–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –Њ–Ї—Б–Є–і–∞. –Я—А–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –і–Є–∞–Љ–µ—В—А –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞ –≤–∞—А—М–Є—А–Њ–≤–∞–ї—Б—П –Њ—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –µ–і–Є–љ–Є—Ж –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–µ—Б—П—В–Ї–Њ–≤ –љ–∞–љ–Њ–Љ–µ—В—А–Њ–≤. –Я–Њ–ї—Г—З–Є–≤—И–µ–µ—Б—П —Б –њ–Њ–Љ–Њ—Й—М—О –і–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –≤–Њ–ї–Њ–Ї–љ–Њ —Б–Њ—Б—В–Њ—П–ї–Њ –Є–Ј –Љ–Њ–љ–Њ–Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Њ–є –Ї—А–µ–Љ–љ–Є–µ–≤–Њ–є —Б–µ—А–і—Ж–µ–≤–Є–љ—Л –Є –Њ–Ї—Б–Є–і–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є —А–∞–Ј–Љ–µ—А–Њ–Љ –њ—А–Є–Љ–µ—А–љ–Њ –≤ –Њ–і–љ—Г —В—А–µ—В—М –і–Є–∞–Љ–µ—В—А–∞. –Ф–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞, —Г—Б—В–Њ–є—З–Є–≤–Њ–≥–Њ –Ї –Њ–Ї–Є—Б–ї–µ–љ–Є—О, –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —Г–і–∞–ї–Є–ї–Є –Њ–Ї—Б–Є–і–љ–Њ–µ –њ–Њ–Ї—А—Л—В–Є–µ –Є –Њ–≥—А–∞–љ–Є—З–Є–ї–Є —А–Њ—Б—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –≤–Њ–ї–Њ–Ї–љ–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –≤–Њ–і–Њ—А–Њ–і–∞. –Ф–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —И–Є—А–Є–љ—Л –Ј–∞–њ—А–µ—Й–µ–љ–љ–Њ–є –Ј–Њ–љ—Л –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞ –±—Л–ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–∞ —Б–Ї–∞–љ–Є—А—Г—О—Й–∞—П —В—Г–љ–љ–µ–ї—М–љ–∞—П —Б–њ–µ–Ї—В—А–Њ—Б–Ї–Њ–њ–Є—П. –Ю–±–љ–∞—А—Г–ґ–Є–ї–Њ—Б—М, —З—В–Њ —И–Є—А–Є–љ–∞ –Ј–Њ–љ—Л —А–∞—Б—В–µ—В —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Ф–Є–∞–Љ–µ—В—А–∞ –≤–Њ–ї–Њ–Ї–љ–∞ вАФ –Њ—В 1,1 —Н–Т –њ—А–Є –і–Є–∞–Љ–µ—В—А–µ 7–љ–Љ –і–Њ 3,5 —Н–Т –њ—А–Є –Ф–Є–∞–Љ–µ—В—А–µ 1,3 –љ–Љ. –≠—В–Њ —Б–Њ–≥–ї–∞—Б—Г–µ—В—Б—П —Б —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–Љ–Є —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–Њ–і–µ–ї—П–Љ–Є –Є —Б–ї—Г–ґ–Є—В —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–Љ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ–Љ –≤–ї–Є—П–љ–Є—П –Ї–≤–∞–љ—В–Њ–≤–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ –њ–ї–Њ—В–љ–Њ—Б—В—М —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –≤ –Ї—А–µ–Љ–љ–Є–µ–≤—Л—Е –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–љ–∞—Е. –£—З–µ–љ—Л–µ –њ–ї–∞–љ–Є—А—Г—О—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –љ–Њ–≤—Л–є –љ–∞–љ–Њ–Љ–∞—В–µ—А–Є–∞–ї –≤ —Б–≤–µ-—В–Њ–і–Є–Њ–і–∞—Е –Є –ї–∞–Ј–µ—А–∞—Е. –Х—Й–µ –Њ–і–љ–Њ–є —Д–Њ—А–Љ–Њ–є –љ–∞–љ–Њ—З–∞—Б—В–Є—Ж –Љ–Њ–≥—Г—В –±—Л—В—М —Б–ї–Њ–Є—Б—В—Л–µ –љ–∞-–љ–Њ—З–µ—И—Г–є–Ї–Є —В–Њ–ї—Й–Є–љ–Њ–є –і–Њ 100 –љ–Љ. –Э–∞ —А–Є—Б. 12 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞-–љ–Њ—З–∞—Б—В–Є—Ж—Л –Љ–Њ–љ—В–Љ–Њ—А–Є–ї–ї–Њ–љ–Є—В–∞ (–≥–ї–Є–љ–Є—Б—В–Њ–≥–Њ –Љ–Є–љ–µ—А–∞–ї–∞ –њ–Њ–і–Ї–ї–∞—Б—Б–∞ —Б–ї–Њ–Є—Б—В—Л—Е —Б–Є–ї–Є–Ї–∞—В–Њ–≤), –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Д—В–Њ—А—Г–≥–ї–µ-—А–Њ–і–љ—Л–Љ–Є —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ–Є —Б–Њ —Б–ї–Њ–Є—Б—В—Л–Љ —Б—В—А–Њ–µ–љ–Є–µ–Љ, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –і–Њ–±–∞–≤–Њ–Ї –Ї –ґ–Є–і–Ї–Є–Љ –њ–Њ–ї–Є–Љ–µ—А–љ—Л–Љ —Б–Є—Б—В–µ–Љ–∞–Љ, –љ–∞–њ—А–Є–Љ–µ—А, –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–≤—В–Њ—Е–Є–Љ–Є–Є. –Ю–і–љ–Є–Љ –Є–Ј –≥–ї–∞–≤–љ—Л—Е —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –Є–љ—В–µ—А–µ—Б—Г—О—В—Б—П —Г—З–µ–љ—Л–µ –≤ –Њ–±–ї–∞—Б—В–Є –љ–∞–љ–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–є, —П–≤–ї—П–µ—В—Б—П —Г–≥–ї–µ—А–Њ–і –Є –µ–≥–Њ –∞–ї–ї–Њ—В—А–Њ–њ–љ—Л–µ —Д–Њ—А–Љ—Л. –Ъ–∞–Ї –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–є —Е–Є–Љ–Є—З–µ—Б–Ї–Є–є —Н–ї–µ–Љ–µ–љ—В —Г–≥–ї–µ—А–Њ–і –±—Л–ї –њ—А–Є–Ј–љ–∞–љ –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Є–Ї–Њ–≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Е–Є–Љ–Є–Є –≤–µ–ї–Є–Ї–Є–Љ —Д—А–∞–љ—Ж—Г–Ј—Б–Ї–Є–Љ —Г—З–µ–љ—Л–Љ –Р–љ—В—Г–∞–љ–Њ–Љ –Ы–Њ—А–∞–љ–Њ–Љ –Ы–∞–≤—Г–∞–Ј—М–µ ( Antoine Laurent Lavoisier) –≤ –Ї–Њ–љ—Ж–µ XVIII –≤–µ–Ї–∞ –Є –њ–Њ–ї—Г—З–Є–ї —Б–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ ( Carboneum) –Њ—В –ї–∞—В–Є–љ—Б–Ї–Њ–≥–Њ —Б–ї–Њ–≤–∞ carbo вАФ —Г–≥–Њ–ї—М. –Ф–Њ –љ–µ–і–∞–≤–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –±—Л–ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г–≥–ї–µ—А–Њ–і –Њ–±—А–∞–Ј—Г–µ—В —З–µ—В—Л—А–µ –∞–ї–ї–Њ—В—А–Њ–њ–љ—Л—Е —Д–Њ—А–Љ—Л вАФ –∞–ї–Љ–∞–Ј, –≥—А–∞—Д–Є—В, –Ї–∞—А–±–Є–љ (–њ–Њ–ї—Г—З–µ–љ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ) –Є –ї–Њ–љ—Б–і–µ–Є–ї–Є—В (–≤–њ–µ—А–≤—Л–µ –љ–∞–є–і–µ–љ –≤ –Љ–µ—В–µ–Њ—А–Є—В–∞—Е, –Ј–∞—В–µ–Љ –њ–Њ–ї—Г—З–µ–љ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ) –Я—А–Є —Н—В–Њ–Љ —Г–ґ–µ –љ–∞ —Н—В–∞–њ–µ –њ–µ—А–µ—Е–Њ–і–∞ —Г–≥–ї–µ—А–Њ–і–∞ –Њ—В –Њ–±—Л–Ї–љ–Њ–≤–µ–љ–љ–Њ–≥–Њ —Г–≥–ї—П (–±–∞–ї–Ї-–Љ–∞—В–µ—А–Є–∞–ї–∞) –і–Њ –≥—А–∞—Д–Є—В–∞ –Њ—В–Љ–µ—З–∞—О—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–≤–Њ–є—Б—В–≤ –Љ–∞—В–µ—А–Є–∞–ї–∞. –С –Ї–Њ–љ—Ж–µ XIX –≤–µ–Ї–∞ –љ–µ–Љ–µ—Ж–Ї–Є–є —Е–Є–Љ–Є–Ї –Р–і–Њ–ї—М—Д —Д–Њ–љ –С–∞–є–µ—А ( Adolf Johann Friedrich Wilhelm von Baeyer) –њ—Л—В–∞–ї—Б—П —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞—В—М –Њ–і–љ–Њ–Љ–µ—А–љ—Л–є (—Ж–µ–њ–Њ—З–µ—З–љ—Л–є) –њ–Њ–ї–Є–Љ–µ—А –Є–Ј –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –∞—Ж–µ—В–Є–ї–µ–љ–∞, –љ–Њ –њ–Њ—В–µ—А–њ–µ–ї –љ–µ—Г–і–∞—З—Г. –£—Б–њ–µ—И–љ—Л–є —Б–Є–љ—В–µ–Ј –Ї–∞—А–±–Є–љ–∞ ( carbyne) –±—Л–ї –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ –≤ –°–Њ–≤–µ—В—Б–Ї–Њ–Љ –°–Њ—О–Ј–µ –Р–ї–µ–Ї—Б–µ–µ–Љ –Ь–Є—Е–∞–є–ї–Њ–≤–Є—З–µ–Љ –°–ї–∞–і–Ї–Њ–≤—Л–Љ, –Ѓ—А–Є–µ–Љ –Я–∞–≤–ї–Њ–≤–Є—З–µ–Љ –Ъ—Г–і—А—П–≤—Ж–µ–≤—Л–Љ, –Т–ї–∞–і–Є–Љ–Є—А–Њ–Љ –Ш–≤–∞–љ–Њ–≤–Є—З–µ–Љ –Ъ–∞—Б–∞—В–Њ—З–Ї–Є–љ—Л–Љ –Є –Т–∞—Б–Є–ї–Є–µ–Љ –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–Є—З–µ–Љ –Ъ–Њ—А—И–∞–Ї–Њ–Љ –≤ –Ш–љ—Б—В–Є—В—Г—В–µ —Н–ї–µ–Љ–µ–љ—В–Њ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –≤ I960 –≥–Њ–і—Г. –°—В—А—Г–Ї—В—Г—А–∞ –Ї–∞—А–±–Є–љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Г–≥–ї–µ—А–Њ–і–љ—Л–µ —Ж–µ–њ–Њ—З–Ї–Є, —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–µ—Б—П –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –і—А—Г–≥ –і—А—Г–≥—Г –Є —Б–≤—П–Ј–∞–љ–љ—Л–µ –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –≤–∞–љ-–і–µ—А-–≤–∞–∞–ї—М—Б–Њ–≤—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Ї–∞—А–±–Є–љ –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞—В—М –≤ –і–≤—Г—Е –Є–Ј–Њ–Љ–µ—А–љ—Л—Е —Д–Њ—А–Љ–∞—Е: 1) –њ–Њ–ї–Є–Є–љ–Њ–≤–Њ–є (—З–µ—А–µ–і–Њ–≤–∞–љ–Є–µ –Њ–і–Є–љ–∞—А–љ—Л—Е –Є —В—А–Њ–є–љ—Л—Е —Б–≤—П–Ј–µ–є): ...-–°=–°-–°=–°-–°=–°-–°=–°... (–∞-–Ї–∞—А–±–Є–љ); 2) –њ–Њ–ї–Є–Ї—Г–Љ—Г–ї–µ–љ–Њ–≤–Њ–є (–≤—Б–µ —Б–≤—П–Ј–Є –і–≤–Њ–є–љ—Л–µ): ...–Ю–°=–°=–°=–°–Ю–°=–°... (|3-–Ї–∞—А–±–Є–љ). –Т 1967 –≥–Њ–і—Г –≤ –Р—А–Є–Ј–Њ–љ—Б–Ї–Њ–Љ –Ї—А–∞—В–µ—А–µ (–°–®–Р), –Њ–±—А–∞–Ј–Њ–≤–∞–≤—И–µ–Љ—Б—П –Њ—В –њ–∞–і–µ–љ–Є—П –≥–Є–≥–∞–љ—В—Б–Ї–Њ–≥–Њ –Љ–µ—В–µ–Њ—А–Є—В–∞, –≤–Љ–µ—Б—В–µ —Б –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–Љ–Є –∞–ї–Љ–∞–Ј–∞–Љ–Є –±—Л–ї–Є –љ–∞–є–і–µ–љ—Л –Є –Ї–Њ—А–Є—З–љ–µ–≤–∞—В–Њ-–ґ–µ–ї—В—Л–µ –Ї—А–Є—Б—В–∞–ї–ї—Л —А–∞–љ–µ–µ –љ–µ–Є–Ј–≤–µ—Б—В–љ–Њ–є –≥–µ–Ї—Б–∞–≥–Њ–љ–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л —Г–≥–ї–µ—А–Њ–і–∞. –Т —З–µ—Б—В—М –∞–љ–≥–ї–Є–є—Б–Ї–Њ–є –ґ–µ–љ—Й–Є–љ—Л-–Ї—А–Є—Б—В–∞–ї–ї–Њ–≥—А–∞—Д–∞ –Ъ—Н—В–ї–Є–љ –Ы–Њ–љ—Б–і–µ–є–ї ( Kathleen Lonsdale) —Н—В–∞ –∞–ї–ї–Њ—В—А–Њ–њ–љ–∞—П —Д–Њ—А–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞ –њ–Њ–ї—Г—З–Є–ї–∞ –љ–∞–Ј–≤–∞–љ–Є–µ ¬Ђ–ї–Њ–љ—Б–і–µ–Є–ї–Є—В¬ї. –Т–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –ї–Њ–љ-—Б–Ф–µ–є–ї–Є—В –±—Л–ї –њ–Њ–ї—Г—З–µ–љ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —В–µ—А–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б–њ–∞–і–∞ –њ–Њ–ї–Є–≥–Є–і—А–Њ–Ї–∞—А–±–Є–љ–∞ –≤ —Б—А–µ–і–µ –∞—А–≥–Њ–љ–∞ –њ—А–Є –∞—В–Љ–Њ—Б—Д–µ—А–Э–Њ–Љ –і–∞–≤–ї–µ–љ–Є–Є –Є –љ–∞–≥—А–µ–≤–µ –≤—Л—И–µ 110 ¬∞–°. –Ш–Ј–≤–µ—Б—В–љ—Л –Є –і—А—Г–≥–Є–µ —Д–Њ—А–Љ—Л —Г–≥–ї–µ—А–Њ–і–∞, –љ–∞–њ—А–Є–Љ–µ—А –∞–Љ–Њ—А—Д–љ—Л–є —Г–≥–ї–µ—А–Њ–і, –±–µ–ї—Л–є —Г–≥–ї–µ—А–Њ–і (—З–∞—А–Њ–Є—В) –Є –і—А., –љ–Њ –Њ–љ–Є —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–њ–Њ–Ј–Є—В–∞–Љ–Є, —В–Њ –µ—Б—В—М —Б–Љ–µ—Б—М—О –Љ–∞–ї—Л—Е —Д—А–∞–≥–Љ–µ–љ—В–Њ–≤ –≥—А–∞—Д–Є—В–∞ –Є –Р—В–Њ–Љ—Л —Г–≥–ї–µ—А–Њ–і–∞ –≤ –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –≥—А–∞—Д–Є—В–∞ (—А–Є—Б. 13, –∞) —Б–≤—П–Ј–∞–љ—Л –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –њ—А–Њ—З–љ—Л–Љ–Є –Ї–Њ–≤–∞–ї–µ–љ—В–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є –Є —Д–Њ—А–Љ–Є—А—Г—О—В —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ—Л–µ –Ї–Њ–ї—М—Ж–∞, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –њ—А–Њ—З–љ—Г—О –Є —Б—В–∞–±–Є–ї—М–љ—Г—О —Б–µ—В–Ї—Г, –њ–Њ—Е–Њ–ґ—Г—О –љ–∞ –њ—З–µ–ї–Є–љ—Л–µ —Б–Њ—В—Л. –°–µ—В–Ї–Є —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –і—А—Г–≥ –љ–∞–і –і—А—Г–≥–Њ–Љ —Б–ї–Њ—П–Љ–Є. –†–∞—Б—Б—В–Њ—П–љ–Є–µ –Љ–µ–ґ–і—Г –∞—В–Њ–Љ–∞–Љ–Є, –љ–∞—Е–Њ–і—П—Й–Є–Љ–Є—Б—П –≤ –≤–µ—А—И–Є–љ–∞—Е –њ—А–∞–≤–Є–ї—М–љ—Л—Е —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤, —А–∞–≤–љ–Њ 0,142 –љ–Љ, –Љ–µ–ґ–і—Г —Б–ї–Њ—П–Љ–Є вАФ 0,335 –љ–Љ. –°–ї–Њ–Є —Б–ї–∞–±–Њ —Б–≤—П–Ј–∞–љ—Л –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є. –Ґ–∞–Ї–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –≥—А–∞—Д–Є—В–∞: –љ–Є–Ј–Ї—Г—О —В–≤–µ—А–і–Њ—Б—В—М –Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –ї–µ–≥–Ї–Њ —А–∞—Б—Б–ї–∞–Є–≤–∞—В—М—Б—П –љ–∞ –Љ–µ–ї—М—З–∞–є—И–Є–µ —З–µ—И—Г–є–Ї–Є, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–Є–ї–Њ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Љ–∞–Ј–Њ—З–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ—В–Є–≤–Њ–Ј–∞–і–Є—А–љ–Њ–≥–Њ –Є –њ—А–Њ-—В–Є–≤–Њ–Є–Ј–љ–Њ—Б–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞. –Т —Б—В—А—Г–Ї—В—Г—А–µ –∞–ї–Љ–∞–Ј–∞ (—А–Є—Б. 13, –±) –Ї–∞–ґ–і—Л–є –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ –≤ —Ж–µ–љ—В—А–µ —В–µ—В—А–∞—Н–і—А–∞, –≤–µ—А—И–Є–љ–∞–Љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–ї—Г–ґ–∞—В —З–µ—В—Л—А–µ –±–ї–Є–ґ–∞–є—И–Є—Е –∞—В–Њ–Љ–∞. –°–Њ—Б–µ–і–љ–Є–µ –∞—В–Њ–Љ—Л —Б–≤—П–Ј–∞–љ—Л –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –Ї–Њ–≤–∞–ї–µ–љ—В–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є. –Ґ–∞–Ї–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В —Б–≤–Њ–є—Б—В–≤–∞ –∞–ї–Љ–∞–Ј–∞ –Ї–∞–Ї –Љ–Є–љ–µ—А–∞–ї–∞ —Б —Б–∞–Љ–Њ–є –≤—Л—Б–Њ–Ї–Њ–є —В–≤–µ—А–і–Њ—Б—В—М—О –Є–Ј –≤—Б–µ—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –≤ –њ—А–Є—А–Њ–і–µ –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤. –£—З–µ–љ—Л–Љ –±—Л–ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ—А–Є –≤—Л—Б–Њ–Ї–Є—Е —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞—Е —Г–≥–ї–µ—А–Њ–і –≤ –≥–∞–Ј–Њ–Њ–±—А–∞–Ј–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Љ–Њ–ґ–µ—В –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М –Ї–ї–∞—Б—В–µ—А—Л (—Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –і–≤—Г—Е –Є–ї–Є –±–Њ–ї–µ–µ –Њ–і–љ–Њ—А–Њ–і–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ (–∞—В–Њ–Љ–Њ–≤ –Є–ї–Є –Љ–Њ–ї–µ–Ї—Г–ї), –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–∞—П –µ–і–Є–љ–Є—Ж–∞, –Њ–±–ї–∞–і–∞—О—Й–∞—П —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є). –Т–µ–ї–Є–Ї–Є–µ –љ–µ–Љ–µ—Ж–Ї–Є–µ —Г—З–µ–љ—Л–µ –Ю—В—В–Њ –У–∞–љ ( Otto Hahn, –Њ—В–Ї—А—Л–≤—И–Є–є –≤ 1938 –≥–Њ–і—Г –і–µ–ї–µ–љ–Є–µ —П–і–µ—А —Г—А–∞–љ–∞, –∞ —В–∞–Ї–ґ–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Н–ї–µ–Љ–µ–љ—В—Л –љ–µ–њ—В—Г–љ–Є–є –Є –њ–ї—Г—В–Њ–љ–Є–є) –Є –§—А–Є—Ж –®—В—А–∞—Б—Б–Љ–∞–љ ( Fritz Strassmann) –≤–њ–µ—А–≤—Л–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ –≤ –њ–∞—А–∞—Е —Г–≥–ї–µ—А–Њ–і–∞, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –≤ —А–∞–≤–љ–Њ–≤–µ—Б–Є–Є —Б –Ї–Њ–љ–і–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–Љ –≥—А–∞—Д–Є—В–Њ–Љ –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞—Е 3000вАФ4000 –Ъ, –њ—А–µ–Њ–±–ї–∞–і–∞—О—В –Ї–ї–∞—Б—В–µ—А—Л –° –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–µ–є—Б—П –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–µ–є –°15. –Ь–µ—В–Њ–і–∞–Љ–Є –Љ–∞—Б—Б-—Б–њ–µ–Ї—В—А–Њ—Б–Ї–Њ–њ–Є–Є –Њ–љ–Є –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ —Г–≥–ї–µ—А–Њ–і–љ—Л–µ –Ї–ї–∞—Б—В–µ—А—Л вАФ –Є–Њ–љ—Л –і–Њ –°+15 вАФ –њ–Њ–ї—Г—З–∞—О—В—Б—П –≤ —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–є –і—Г–≥–µ –Љ–µ–ґ–і—Г –≥—А–∞—Д–Є—В–Њ–≤—Л–Љ–Є —Н–ї–µ–Ї—В—А–Њ–і–∞–Љ–Є. –Я–µ—А–≤—Л–µ –Ї–≤–∞–љ—В–Њ–≤—Л–µ —А–∞—Б—З–µ—В—Л —Б—В—А—Г–Ї—В—Г—А —Г–≥–ї–µ—А–Њ–і–љ—Л—Е –Ї–ї–∞—Б—В–µ—А–Њ–≤ –і–Њ 20 –∞—В–Њ–Љ–Њ–≤ –±—Л–ї–Є —Б–і–µ–ї–∞–љ—Л –≤ 1959 –≥–Њ–і—Г. –£—З–µ–љ—Л–µ –њ—А–Є—И–ї–Є –Ї –≤—Л–≤–Њ–і—Г, —З—В–Њ —В–∞–Ї–Є–µ –Ї–ї–∞—Б—В–µ—А—Л –Є–Љ–µ—О—В –≤–Є–і –ї–Є–љ–µ–є–љ—Л—Е —Ж–µ–њ–µ–є –Њ—В –°2, –і–Њ –°10, –∞ –њ—А–Є –±–Њ–ї—М—И–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –∞—В–Њ–Љ–Њ–≤ –і–Њ–ї–ґ–љ—Л –њ—А–Є–Њ–±—А–µ—В–∞—В—М –Ї–Њ–ї—М—Ж–µ–Њ–±—А–∞–Ј–љ—Г—О —Д–Њ—А–Љ—Г. –Я—А–Є –і–∞–ї—М–љ–µ–є—И–µ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Г–≥–ї–µ—А–Њ–і–љ—Л—Е –∞—В–Њ–Љ–Њ–≤ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ–µ—А–Є–Њ–і –Љ–Њ–≥—Г—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М—Б—П –і–≤—Г—Е - –Є —В—А–µ—Е–Љ–µ—А–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л. –Т–Њ–њ—А–Њ—Б –Њ —В–Њ–Љ, –Ї–∞–Ї—Г—О –ґ–µ —Д–Њ—А–Љ—Г –Њ–љ–Є –Є–Љ–µ—О—В –љ–∞ —Б–∞–Љ–Њ–Љ –і–µ–ї–µ, –і–Њ–ї–≥–Њ –Њ—Б—В–∞–≤–∞–ї—Б—П –і–Є—Б–Ї—Г—Б—Б–Є–Њ–љ–љ—Л–Љ. –Э–∞–њ—А–Є–Љ–µ—А, –≤ —Б–µ—А–µ–і–Є–љ–µ 60-—Е –≥–Њ–і–Њ–≤ –∞–љ–≥–ї–Є–є—Б–Ї–Є–є —Е–Є–Љ–Є–Ї-—В–µ–Њ—А–µ—В–Є–Ї –Ф–ґ–Њ–љ-–≠–і–≤–∞—А–і –Ы–µ–љ–љ–∞—А–і-–Ф–ґ–Њ–љ—Б ( John Edward Lennard - Johnes) –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є–ї, —З—В–Њ –≥—А–∞—Д–Є—В–Њ–≤—Л–µ –ї–Є—Б—В—Л –Љ–Њ–≥—Г—В —Б–≤–Њ—А–∞—З–Є–≤–∞—В—М—Б—П, –Њ–±—А–∞–Ј—Г—П ¬Ђ–њ–Њ–ї—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л¬ї. –£–≥–ї–µ—А–Њ–і–љ—Л–µ –Ї–ї–∞—Б—В–µ—А—Л –≤–њ–µ—А–≤—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ 1984 –≥–Њ–і—Г, –∞ —Б–∞–Љ–∞ –Љ–Њ–ї–µ–Ї—Г–ї–∞ –°60, –Ї–∞–Ї —Г–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М, –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –≤ 1985 –≥–Њ–і—Г –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–∞—Б—Б-—Б–њ–µ–Ї—В—А–Њ–≤ –њ–∞—А–Њ–≤ –≥—А–∞—Д–Є—В–∞ –њ–Њ—Б–ї–µ –ї–∞–Ј–µ—А–љ–Њ–≥–Њ –Њ–±–ї—Г—З–µ–љ–Є—П —В–≤–µ—А–і–Њ–≥–Њ –Њ–±—А–∞–Ј—Ж–∞. –Ґ–∞–Ї —Б—В–∞–ї–∞ –Є–Ј–≤–µ—Б—В–љ–∞ –µ—Й–µ –Њ–і–љ–∞ –∞–ї–ї–Њ—В—А–Њ–њ–љ–∞—П —Д–Њ—А–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞, —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є ¬Ђ—Д—Г–ї–ї–µ—А–µ–љ¬ї (–Љ–љ–Њ–≥–Њ–∞—В–Њ–Љ–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л —Г–≥–ї–µ—А–Њ–і–∞ –°–њ). –Э–∞–Ј–≤–∞–љ–Є–µ –і–∞–љ–Њ –≤ —З–µ—Б—В—М –Є–Ј–≤–µ—Б—В–љ–Њ–≥–Њ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–≥–Њ –∞—А—Е–Є—В–µ–Ї—В–Њ—А–∞-–∞–≤–∞–љ–≥–∞—А–і–Є—Б—В–∞, —Д–Є–ї–Њ—Б–Њ—Д–∞, –њ–Њ—Н—В–∞ –Є –Є–љ–ґ–µ–љ–µ—А–∞ –†–Є—З–∞—А–і–∞ –С–∞–Ї–Љ–Є–љ-—Б—В–µ—А–∞ –§—Г–ї–ї–µ—А–∞ ( Richard Buckminster Fuller), —А–∞–Ј—А–∞–±–Њ—В–∞–≤—И–µ–≥–Њ –Ф–Є–Ј–∞–є–љ —Б—В—А–Њ–Є—В–µ–ї—М–љ—Л—Е –Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–є, —Д–Њ—А–Љ–∞ –Ї–Њ—В–Њ—А—Л—Е –∞–љ–∞–ї–Њ–≥–Є—З–љ–∞ —Д–Њ—А–Љ–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л —Д—Г–ї–ї–µ—А–µ–љ–∞ –°60 (—А–Є—Б. 13, –≤). –Я–Њ —Б—Г—Й–µ—Б—В–≤—Г —Д—Г–ї–ї–µ—А–µ–љ вАФ –љ–Њ–≤–∞—П —Д–Њ—А–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞. –Ь–Њ–ї–µ–Ї—Г–ї–∞ –°60 —Б–Њ–і–µ—А–ґ–Є—В —Д—А–∞–≥–Љ–µ–љ—В—Л —Б –њ—П—В–Є–Ї—А–∞—В–љ–Њ–є —Б–Є–Љ–Љ–µ—В—А–Є–µ–є, –љ–µ—Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ–є –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П–Љ –≤ –њ—А–Є—А–Њ–і–µ. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є–Ј–љ–∞–љ–Њ, —З—В–Њ –Љ–Њ–ї–µ–Ї—Г–ї–∞ —Д—Г–ї–ї–µ—А–µ–љ–∞ —П–≤–ї—П–µ—В—Б—П –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї–Њ–є, –∞ –Ї—А–Є—Б—В–∞–ї–ї, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–є —В–∞–Ї–Є–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є (—Д—Г–ї–ї–µ—А–Є—В), вАФ —Н—В–Њ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–є –Ї—А–Є—Б—В–∞–ї–ї, —П–≤–ї—П—О—Й–Є–є—Б—П —Б–≤—П–Ј—Г—О—Й–Є–Љ –Ј–≤–µ–љ–Њ–Љ –Љ–µ–ґ–і—Г –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ –Є –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ. –Ш–Ј –њ—А–∞–≤–Є–ї—М–љ—Л—Е —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤ –ї–µ–≥–Ї–Њ –≤—Л–ї–Њ–ґ–Є—В—М –њ–ї–Њ—Б–Ї—Г—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М, –Њ–і–љ–∞–Ї–Њ –љ–µ–ї—М–Ј—П —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М –Ј–∞–Љ–Ї–љ—Г—В—Г—О. –Ф–ї—П —Н—В–Њ–≥–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞–Ј—А–µ–Ј–∞—В—М —З–∞—Б—В—М —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ—Л—Е –Ї–Њ–ї–µ—Ж –Є –Є–Ј —А–∞–Ј—А–µ–Ј–∞–љ–љ—Л—Е —З–∞—Б—В–µ–є –њ–Њ—Б—В—А–Њ–Є—В—М –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Є. –Т —Д—Г–ї–ї–µ-—А–µ–љ–µ –њ–ї–Њ—Б–Ї–∞—П —Б–µ—В–Ї–∞ —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤ (–≥—А–∞—Д–Є—В–Њ–≤–∞—П —Б–µ—В–Ї–∞) —Б–≤–µ—А–љ—Г—В–∞ –Є —Б—И–Є—В–∞ –≤ –Ј–∞–Љ–Ї–љ—Г—В—Г—О —Б—Д–µ—А—Г. –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В—М —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤ —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –≤ –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Є. –Ю–±—А–∞–Ј—Г–µ—В—Б—П —Г—Б–µ—З–µ–љ–љ—Л–є –Є–Ї–Њ—Б–∞—Н–і—А —Б –і–µ—Б—П—В—М—О –Њ—Б—П–Љ–Є —Б–Є–Љ–Љ–µ—В—А–Є–Є —В—А–µ—В—М–µ–≥–Њ –њ–Њ—А—П–і–Ї–∞ –Є —И–µ—Б—В—М—О –Њ—Б—П–Љ–Є —Б–Є–Љ–Љ–µ—В—А–Є–Є –њ—П—В–Њ–≥–Њ –њ–Њ—А—П–і–Ї–∞. –£ –Ї–∞–ґ–і–Њ–є –≤–µ—А—И–Є–љ—Л —Н—В–Њ–є —Д–Є–≥—Г—А—Л –µ—Б—В—М —В—А–Є –±–ї–Є–ґ–∞–є—И–Є—Е —Б–Њ—Б–µ–і–∞. –Ъ–∞–ґ–і—Л–є —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї –≥—А–∞–љ–Є—З–Є—В —Б —В—А–µ–Љ—П —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞–Љ–Є –Є —В—А–µ–Љ—П –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞–Љ–Є, –∞ –Ї–∞–ґ–і—Л–є –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї вАФ —В–Њ–ї—М–Ї–Њ —Б —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞–Љ–Є. –Ъ–∞–ґ–і—Л–є –∞—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ –°–±0 –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –≤–µ—А—И–Є–љ–∞—Е –і–≤—Г—Е —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤ –Є –Њ–і–љ–Њ–≥–Њ –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞ –Є –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–µ–Њ—В–ї–Є—З–Є–Љ –Њ—В –і—А—Г–≥–Є—Е –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞. –Р—В–Њ–Љ—Л —Г–≥–ї–µ—А–Њ–і–∞, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ —Б—Д–µ—А—Г, —Б–≤—П–Ј–∞–љ—Л –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є —Б–Є–ї—М–љ–Њ–є –Ї–Њ–≤–∞–ї–µ–љ—В–љ–Њ–є —Б–≤—П–Ј—М—О. –Ґ–Њ–ї—Й–Є–љ–∞ —Б—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є вАФ 0,1 –љ–Љ, —А–∞–і–Є—Г—Б –Љ–Њ–ї–µ–Ї—Г–ї—Л –°60 вАФ 0,357 –љ–Љ. –Ф–ї–Є–љ–∞ —Б–≤—П–Ј–Є –Ю–° –≤ –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–µ вАФ 0,143 –љ–Љ, –≤ —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–µ вАФ 0,139 –љ–Љ. –Ь–Њ–ї–µ–Ї—Г–ї—Л –≤—Л—Б—И–Є—Е —Д—Г–ї–ї–µ—А–µ–љ–Њ–≤ –°70, –°74, –°76, –°84, –°164, –°192, –°21–± —В–∞–Ї–ґ–µ –Є–Љ–µ—О—В —Д–Њ—А–Љ—Г –Ј–∞–Љ–Ї–љ—Г—В–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є. –§—Г–ї–ї–µ—А–µ–љ—Л —Б –њ < 60 –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –љ–µ—Г—Б—В–Њ–є—З–Є–≤—Л–Љ–Є, —Е–Њ—В—П –Є–Ј —З–Є—Б—В–Њ —В–Њ–њ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ–Њ–±—А–∞–ґ–µ–љ–Є–є –љ–∞–Є–Љ–µ–љ—М—И–Є–є –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е —Д—Г–ї–ї–µ—А–µ–љ–Њ–≤ вАФ –њ—А–∞–≤–Є–ї—М–љ—Л–є –і–Њ–і–µ–Ї–∞—Н–і—А –°20. –Ъ—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є —Д—Г–ї–ї–µ—А–µ–љ, –Ї–Њ—В–Њ—А—Л–є –±—Л–ї –љ–∞–Ј–≤–∞–љ —Д—Г–ї–ї–µ-—А–Є—В–Њ–Љ, –Є–Љ–µ–µ—В –≥—А–∞–љ–µ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Г—О –Ї—Г–±–Є—З–µ—Б–Ї—Г—О (–У–¶–Ъ) —А–µ—И–µ—В–Ї—Г –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–є –≥—А—Г–њ–њ—Л —Б –њ–∞—А–∞–Љ–µ—В—А–Њ–Љ –Ї—Г–±–Є—З–µ—Б–Ї–Њ–є —А–µ—И–µ—В–Ї–Є –∞–Њ = 1,42 –љ–Љ, —А–∞—Б—Б—В–Њ—П–љ–Є–µ–Љ –Љ–µ–ґ–і—Г –±–ї–Є–ґ–∞–є—И–Є–Љ–Є —Б–Њ—Б–µ–і—П–Љ–Є 1 –љ–Љ –Є —З–Є—Б–ї–Њ–Љ –±–ї–Є–ґ–∞–є—И–Є—Е —Б–Њ—Б–µ–і–µ–є –≤ –У–¶–Ъ-—А–µ—И–µ—В–Ї–µ —Д—Г–ї-–ї–µ—А–Є—В–∞, —А–∞–≤–љ—Л–Љ 12. –Ь–µ–ґ–і—Г –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –°60 –≤ –Ї—А–Є—Б—В–∞–ї–ї–µ —Д—Г–ї–ї–µ—А–Є—В–∞ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —Б–ї–∞–±–∞—П —Б–≤—П–Ј—М –Т–∞–љ-–і–µ—А-–Т–∞–∞–ї—М—Б–∞. –Ь–µ—В–Њ–і–Њ–Љ —П–і–µ—А–љ–Њ–≥–Њ –Љ–∞–≥–љ–Є—В–љ–Њ–≥–Њ —А–µ–Ј–Њ–љ–∞–љ—Б–∞ –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л –°60 –≤—А–∞—Й–∞—О—В—Б—П –≤–Њ–Ї—А—Г–≥ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П —А–∞–≤–љ–Њ–≤–µ—Б–Є—П —Б —З–∞—Б—В–Њ—В–Њ–є 1012 —Б 1. –Я—А–Є –њ–Њ–љ–Є–ґ–µ–љ–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –≤—А–∞—Й–µ–љ–Є–µ –Ј–∞–Љ–µ–і–ї—П–µ—В—Б—П. –Я—А–Є 249 –Ъ –≤ —Д—Г–ї–ї–µ—А–Є—В–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Д–∞–Ј–Њ–≤—Л–є –њ–µ—А–µ—Е–Њ–і –њ–µ—А–≤–Њ–≥–Њ —А–Њ–і–∞, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –≥—А–∞–љ–µ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–∞—П —А–µ—И–µ—В–Ї–∞ –њ–µ—А–µ—Е–Њ–і–Є—В –≤ –њ—А–Њ—Б—В—Г—О –Ї—Г–±–Є—З–µ—Б–Ї—Г—О. –Я—А–Є —Н—В–Њ–Љ –Њ–±—К–µ–Љ —Д—Г–ї–ї–µ—А–Є—В–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –љ–∞ 1%. –Ъ—А–Є—Б—В–∞–ї–ї —Д—Г–ї–ї–µ—А–Є—В–∞ –Є–Љ–µ–µ—В —Г–і–µ–ї—М–љ—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М 1,7 –≥/—Б–Љ3, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є –≥—А–∞—Д–Є—В–∞ (2,3 –≥/—Б–Љ3) –Є –∞–ї–Љ–∞–Ј–∞ (3,5 –≥/—Б–Љ3). –Ь–Њ–ї–µ–Ї—Г–ї–∞ –°–±0 —Б–Њ—Е—А–∞–љ—П–µ—В —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М –≤ –Є–љ–µ—А—В–љ–Њ–є –∞—В–Љ–Њ—Б—Д–µ—А–µ –∞—А–≥–Њ–љ–∞ –і–Њ —В–µ–Љ–њ–µ—А–∞—В—Г—А –њ–Њ—А—П–і–Ї–∞ 1700 –Ъ. –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞ —Г–ґ–µ –њ—А–Є 500 –Ъ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Њ–Ї–Є—Б–ї–µ–љ–Є–µ —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –Њ–Ї—Б–Є–і–∞ –°–Ю –Є –і–Є–Њ–Ї—Б–Є–і–∞ —Г–≥–ї–µ—А–Њ–і–∞ –°–Ю2. –Я—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–Є –Њ–±–ї—Г—З–µ–љ–Є–Є —Д–Њ—В–Њ–љ–∞–Љ–Є —Б —Н–љ–µ—А–≥–Є–µ–є –≤—Б–µ–≥–Њ –≤ 0,55 —Н–Т, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–Є–ґ–µ —Н–љ–µ—А–≥–Є–Є —Д–Њ—В–Њ–љ–Њ–≤ –≤–Є–і–Є–Љ–Њ–≥–Њ —Б–≤–µ—В–∞ 1,54 —Н–Т. –Т—Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Њ–≥–Њ —З–Є—Б—В—Л–є —Д—Г–ї–ї–µ—А–Є—В —В—А–µ–±—Г–µ—В —Е—А–∞–љ–µ–љ–Є—П –≤ —В–µ–Љ–љ–Њ—В–µ. –Я—А–Њ—Ж–µ—Б—Б, –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–Є–є—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —З–∞—Б–Њ–≤, –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј—А—Г—И–µ–љ–Є—О –У–¶–Ъ-—А–µ—И–µ—В-–Ї–Є —Д—Г–ї–ї–µ—А–Є—В–∞ –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –љ–µ—Г–њ–Њ—А—П–і–Њ—З–µ–љ–љ–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л, –≤ –Ї–Њ—В–Њ—А–Њ–є –љ–∞ –Є—Б—Е–Њ–і–љ—Г—О –Љ–Њ–ї–µ–Ї—Г–ї—Г –°60 –њ—А–Є—Е–Њ–і–Є—В—Б—П 12 –∞—В–Њ–Љ–Њ–≤ –Ї–Є—Б–ї–Њ—А–Њ–і–∞. –Я—А–Є —Н—В–Њ–Љ —Д—Г–ї–ї–µ—А–µ–љ—Л –њ–Њ–ї–љ–Њ—Б—В—М—О —В–µ—А—П—О—В —Б–≤–Њ—О —Д–Њ—А–Љ—Г. –Я–Њ —Б–Њ–Њ–±—Й–µ–љ–Є—О physorg. com —Б–Њ —Б—Б—Л–ї–Ї–Њ–є –љ–∞ –Њ–љ–ї–∞–є–љ–Њ–≤—Г—О –њ—Г–±–ї–Є–Ї–∞—Ж–Є—О –≤ Proceedings of the National Academy of Sciences, –њ–µ—А–≤—Л–є –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Њ–≥ —Д—Г–ї–ї–µ—А–µ–љ–∞ —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ –≤ –Ґ–Є—Е–Њ–Њ–Ї–µ–∞–љ—Б–Ї–Њ–є —Б–µ–≤–µ—А–Њ-–Ј–∞–њ–∞–і–љ–Њ–є –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ь–Є–љ–Є—Б—В–µ—А—Б—В–≤–∞ —Н–љ–µ—А–≥–µ—В–Є–Ї–Є –°–®–Р –≤ 2006 –≥–Њ–і—Г. –Я—А–Є —Н—В–Њ–Љ —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—З–µ—В—Л –Я—А–Њ–≤–Њ–і–Є–ї–∞ –≥—А—Г–њ–њ–∞ –њ—А–Њ—Д–µ—Б—Б–Њ—А–∞ –°—П–Њ –І—Н–љ –¶–Ј–µ–љ–∞ ( Xiao Cheng Zeng) –Є–Ј –£–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ —И—В–∞—В–∞ –Э–µ–±—А–∞—Б–Ї–∞, –Ы–Є–љ–Ї–Њ–ї—М–љ. –°–∞–Љ–∞—П –Љ–∞–ї–∞—П –Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї —Б–Њ—Б—В–Њ–Є—В –≤—Б–µ–≥–Њ –Є–Ј 16 –∞—В–Њ–Љ–Њ–≤ –Ј–Њ–ї–Њ—В–∞ –Є –њ–Њ –≤–Є–і—Г –±–Њ–ї—М—И–µ –њ–Њ—Е–Њ–ґ–∞ –љ–∞ –і—А–∞–≥–Њ—Ж–µ–љ–љ—Л–є –Ї–∞–Љ–µ–љ—М, —З–µ–Љ –љ–∞ —И–∞—А (—А–Є—Б. 14), вАФ –њ–Њ —Б—Г—Й–µ—Б—В–≤—Г, —Н—В–Њ –њ–µ—А–≤—Л–µ –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–µ –њ–Њ–ї—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л. –Х—Б–ї–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ —З–Є—Б–ї–Њ –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П –њ–Њ–ї–Њ–є –Ј–∞–Љ–Ї–љ—Г—В–Њ–є –Љ–Њ–ї–µ–Ї—Г–ї—Л, 60, —В–Њ –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П –∞–љ–∞–ї–Њ–≥–∞ –Є–Ј –Ј–Њ–ї–Њ—В–∞ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –љ–∞–Љ–љ–Њ–≥–Њ –Љ–µ–љ—М—И–µ –∞—В–Њ–Љ–Њ–≤. –Я–Њ —Б–ї–Њ–≤–∞–Љ —А—Г–Ї–Њ–≤–Њ–і–Є—В–µ–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ—Д–µ—Б—Б–Њ—А–∞ —Д–Є–Ј–Є–Ї–Є –Є–Ј –£–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ —И—В–∞—В–∞ –Т–∞—И–Є–љ–≥—В–Њ–љ –Ы–∞–є-–®—Н–љ –Т–∞–љ ( Lai - Sheng Wang), —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –Љ–Њ–ї–µ–Ї—Г–ї—Л —Б–Њ—Б—В–Њ—П—В –Є–Ј 16, 17 –Є 18 –∞—В–Њ–Љ–Њ–≤ –Ј–Њ–ї–Њ—В–∞. –Ю–љ–Є –Њ–±—А–∞–Ј—Г—О—В —В—А–µ—Г–≥–Њ–ї—М–љ–Є–Ї–Є, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –Є —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л. –Ь–Њ–ї–µ–Ї—Г–ї—Г –Р–Є16 –њ–Њ–ї—Г—З–∞—О—В –Ј–∞ —Б—З–µ—В –Є–Ј—К—П—В–Є—П —З–µ—В—Л—А–µ—Е —Г–≥–ї–Њ–≤—Л—Е –∞—В–Њ–Љ–Њ–≤ –Ј–Њ–ї–Њ—В–∞ –Є–Ј –љ–µ–њ–Њ–ї–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л –Р–Є20 –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –њ–Њ–і–Њ–≥—А–µ–≤–∞ –Њ—Б—В–∞–≤—И–µ–є—Б—П —Б—В—А—Г–Ї—В—Г—А—Л. –Ъ–Њ–≥–і–∞ —Б–Њ–Њ–±—Й–µ–љ–љ–∞—П —Б–Є—Б—В–µ–Љ–µ —Н–љ–µ—А–≥–Є—П –њ—А–µ–≤—Л—И–∞–µ—В —Н–љ–µ—А–≥–Є—О –∞–Ї—В–Є–≤–∞—Ж–Є–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Г—О –і–ї—П –њ–µ—А–µ—Б—В—А–Њ–є–Ї–Є, –∞—В–Њ–Љ—Л —Б–∞–Љ–Є –≤—Л—Б—В—А–∞–Є–≤–∞—О—В—Б—П –≤ –љ–∞–Є–±–Њ–ї–µ–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є –≤—Л–≥–Њ–і–љ—Г—О —Б—В—А—Г–Ї—В—Г—А—Г. –Э–∞—А—П–і—Г —Б–Њ —Б—Д–µ—А–Њ–Є–і–∞–ї—М–љ—Л–Љ–Є —Г–≥–ї–µ—А–Њ–і–љ—Л–Љ–Є —Б—В—А—Г–Ї—В—Г—А–∞–Љ–Є –Љ–Њ–≥—Г—В —В–∞–Ї–ґ–µ –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М—Б—П –њ—А–Њ—В—П–ґ–µ–љ–љ—Л–µ —Ж–Є–ї–Є–љ–і—А–Є—З–µ—Б–Ї–Є–µ —Б—В—А—Г–Ї—В—Г—А—Л, —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –њ–∞–љ–Њ—В—А—Г–±–Ї–Є, –Њ—В–Ї—А—Л—В—Л–µ –≤ –Ї–∞–Ї–Њ–є-—В–Њ —Б—В–µ–њ–µ–љ–Є —Б–ї—Г—З–∞–є–љ–Њ –≤ 1991 –≥–Њ–і—Г –°. –Ш–Є–і–ґ–Є–Љ–Њ–є –Є –Њ—В–ї–Є—З–∞—О—Й–Є–µ—Б—П —И–Є—А–Њ–Ї–Є–Љ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ–Љ —Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤. –Ш–і–µ–∞–ї—М–љ–∞—П —Г–≥–ї–µ—А–Њ–і–љ–∞—П –љ–∞–љ–Њ—В—А—Г–±–Ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Ж–Є–ї–Є–љ–і—А, –њ–Њ–ї—Г—З–µ–љ–љ—Л–є –њ—А–Є —Б–≤–Њ—А–∞—З–Є–≤–∞–љ–Є–Є –≥—А–∞—Д–µ–љ–Њ–≤–Њ–є –њ–ї–Њ—Б–Ї–Њ—Б—В–Є, —В–Њ –µ—Б—В—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М, –≤—Л–ї–Њ–ґ–µ–љ–љ—Г—О –њ—А–∞–≤–Є–ї—М–љ—Л–Љ–Є —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞–Љ–Є, –≤ –≤–µ—А—И–Є–љ–∞—Е –Ї–Њ—В–Њ—А—Л—Е —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ—Л –∞—В–Њ–Љ—Л —Г–≥–ї–µ—А–Њ–і–∞ (—А–Є—Б. 15). –У—А–∞—Д–µ–љ вАФ —А–∞–Ј–≤–µ—А–љ—Г—В–∞—П –≤ –і–≤—Г—Е–Љ–µ—А–љ—Л–є –ї–Є—Б—В –љ–∞–љ–Њ—В—А—Г–±–Ї–∞. –≠—В–Њ—В –љ–∞–љ–Њ–Љ–∞—В–µ—А–Є–∞–ї –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –њ–ї–µ–љ–Ї—Г –Є–Ј –∞—В–Њ–Љ–Њ–≤ —Г–≥–ї–µ—А–Њ–і–∞, —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –Њ–і–љ—Г –Љ–Њ–ї–µ–Ї—Г–ї—Г. –Э–Њ–≤—Л–є –Љ–∞—В–µ—А–Є–∞–ї –љ–∞–Ј–≤–∞–љ –і–≤—Г—Е–Љ–µ—А–љ—Л–Љ —Д—Г–ї–ї–µ—А–µ–љ–Њ–Љ. –У—А–∞—Д–µ–љ —Б—В–∞–±–Є–ї–µ–љ, –Њ—З–µ–љ—М –≥–Є–±–Њ–Ї, –њ—А–Њ—З–µ–љ –Є –њ—А–Њ–≤–Њ–і–Є—В —Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Є–є —В–Њ–Ї. –С–ї–∞–≥–Њ–і–∞—А—П —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ —Г–≥–ї–µ—А–Њ–і–∞ –≤ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–є —А–µ—И–µ—В–Ї–µ –≥—А–∞—Д–µ–љ–∞ –Њ–љ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є –Љ–Њ–±–Є–ї—М–љ–Њ—Б—В—М—О —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤, —З—В–Њ –і–µ–ї–∞–µ—В –≥—А–∞—Д–µ–љ –Њ—З–µ–љ—М –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ–є –Њ—Б–љ–Њ–≤–Њ–є –љ–∞-–љ–Њ—Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е —Г—Б—В—А–Њ–є—Б—В–≤. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В —Д—Г–ї–ї–µ—А–µ–љ–Њ–≤ –љ–∞–љ–Њ—В—А—Г–±–Ї–Є –Љ–Њ–≥—Г—В —Б–Њ–і–µ—А–ґ–∞—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–ї–Њ–µ–≤. –Э–∞–±–ї—О–і–µ–љ–Є—П, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–µ —Б –њ–Њ–Љ–Њ—Й—М—О —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Њ–≤, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –љ–∞-–љ–Њ—В—А—Г–±–Њ–Ї —Б–Њ—Б—В–Њ—П—В –Є–Ј –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –≥—А–∞—Д–µ–љ–Њ–≤—Л—Е —Б–ї–Њ–µ–≤, –ї–Є–±–Њ –≤–ї–Њ–ґ–µ–љ–љ—Л—Е –Њ–і–Є–љ –≤ –і—А—Г–≥–Њ–є, –ї–Є–±–Њ –љ–∞–≤–Є—В—Л—Е –љ–∞ –Њ–±—Й—Г—О –Њ—Б—М. –Ґ–∞–Ї–Є–µ –Љ–љ–Њ–≥–Њ—Б–ї–Њ–є–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –њ–Њ–ї—Г—З–Є–ї–Є –љ–∞–Ј–≤–∞–љ–Є—П ¬Ђ–ї—Г–Ї–Њ–≤–Є—З–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л¬ї вАФ –Њ–љ–Є–Њ–љ—Л (–∞–љ–≥–ї. onion вАФ –ї—Г–Ї–Њ–≤–Є—Ж–∞). –≠—В–Њ –Њ—З–µ–љ—М —Б–ї–Њ–ґ–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –і–∞–ґ–µ –љ–µ –Є–Љ–µ—В—М —Б–Є–Љ–Љ–µ—В—А–Є–Є. –С–Њ–ї—М—И–Є–µ –Ї—Г—Б–Ї–Є —В–∞–Ї–Є—Е ¬Ђ–≥–Є–≥–∞–љ—В—Б–Ї–Є—Е¬ї —Д—Г–ї–ї–µ—А–µ–љ–Њ–≤ –≥—А–∞-—Д–Є—В–Є–Ј–Є—А–Њ–≤–∞–љ—Л, –∞ —А–∞—Б—Б—В–Њ—П–љ–Є–µ –Љ–µ–ґ–і—Г —Б–ї–Њ—П–Љ–Є –±–ї–Є–Ј–Ї–Њ –Ї —А–∞—Б—Б—В–Њ—П–љ–Є—О –Љ–µ–ґ–і—Г —Г–≥–ї–µ—А–Њ–і–љ—Л–Љ–Є —Б–ї–Њ—П–Љ–Є –≤ –≥—А–∞—Д–Є—В–µ (0,33 –љ–Љ). –Я–Њ–і–Њ–±–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –≤–ї–Њ–ґ–µ–љ–Є–µ–Љ –і—А—Г–≥ –≤ –і—А—Г–≥–∞ (–Ї–∞–Ї –≤ –Љ–∞—В—А–µ—И–Ї–µ) –Љ–Њ–ї–µ–Ї—Г–ї –°60, –°240> –°960, –°1500, –°21–±0, –°2940 –Є —В.–і. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –і–ї—П –њ–Њ–і–Њ–±–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –Є–Љ–µ—О—В—Б—П –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–µ –≤–Є–і—Л —Б–Є–Љ–Љ–µ—В—А–Є–Є вАФ –ї–Є–±–Њ —Б—Д–µ—А–Є—З–µ—Б–Ї–∞—П —Б–Є–Љ–Љ–µ—В—А–Є—П, –ї–Є–±–Њ —Б–Є–Љ–Љ–µ—В—А–Є—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Њ—Б–Є –њ—П—В–Њ–≥–Њ –њ–Њ—А—П–і–Ї–∞. –І–µ–Љ –±–Њ–ї—М—И–µ —А–∞–Ј–Љ–µ—А—Л —З–∞—Б—В–Є—Ж—Л, —В–µ–Љ —П—А—З–µ –≤—Л—А–∞–ґ–µ–љ —Н—В–Њ—В —Н—Д—Д–µ–Ї—В. –Я–Њ–і–Њ–±–љ—Л–µ —Б—В—А—Г–Ї—В—Г—А—Л –Њ–±—А–∞–Ј—Г—О—В—Б—П –≤ —Б–ї—Г—З–∞–µ –Ј–∞–Љ–µ—Й–µ–љ–Є—П —Б—В—А—Г–Ї—В—Г—А —Б –љ–µ–љ—Г–ї–µ–≤–Њ–є –Ї—А–Є–≤–Є–Ј–љ–Њ–є (–њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Є –≤ –Њ–±—Л—З–љ—Л—Е —Д—Г–ї–ї–µ—А–µ–љ–∞—Е) –љ–∞ –≥—А–∞—Д–Є—В–Њ–≤—Л–µ —Б–ї–Њ–Є. –°—В—А—Г–Ї—В—Г—А–∞ –Њ–і–љ–Њ—Б–ї–Њ–є–љ—Л—Е –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї, –љ–∞–±–ї—О–і–∞–µ–Љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ, –≤–Њ –Љ–љ–Њ–≥–Є—Е –Њ—В–љ–Њ—И–µ–љ–Є—П—Е –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ–Њ–є –≤—Л—И–µ –Є–і–µ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –Љ–Њ–і–µ–ї–Є. –Я—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Н—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –≤–µ—А—И–Є–љ –љ–∞–љ–Њ—В—А—Г–±–Ї–Є, —Д–Њ—А–Љ–∞ –Ї–Њ—В–Њ—А—Л—Е, –Ї–∞–Ї —Б–ї–µ–і—Г–µ—В –Є–Ј –љ–∞–±–ї—О–і–µ–љ–Є–є, –і–∞–ї–µ–Ї–∞ –Њ—В –Є–і–µ–∞–ї—М–љ–Њ–є –њ–Њ–ї—Г—Б—Д–µ—А—Л. –Ґ–∞–Ї–∞—П —В—А—Г–±–Ї–∞ –Ј–∞–Ї–∞–љ—З–Є–≤–∞–µ—В—Б—П –њ–Њ–ї—Г—Б—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ–Є –≤–µ—А—И–Є–љ–∞–Љ–Є, —Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ–Є –љ–∞—А—П–і—Г —Б –њ—А–∞–≤–Є–ї—М–љ—Л–Љ–Є —И–µ—Б—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–∞–Љ–Є –њ–Њ —И–µ—Б—В—М –њ—А–∞–≤–Є–ї—М–љ—Л—Е –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤. –Э–∞–ї–Є—З–Є–µ –њ—П—В–Є—Г–≥–Њ–ї—М–љ–Є–Ї–Њ–≤ –љ–∞ –Ї–Њ–љ—Ж–∞—Е —В—А—Г–±–Њ–Ї –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Є—Е –Ї–∞–Ї –њ—А–µ–і–µ–ї—М–љ—Л–є —Б–ї—Г—З–∞–є –Љ–Њ–ї–µ–Ї—Г–ї —Д—Г–ї–ї–µ—А–µ–љ–Њ–≤, –і–ї–Є–љ–∞ –њ—А–Њ–і–Њ–ї—М–љ–Њ–є –Њ—Б–Є –Ї–Њ—В–Њ—А—Л—Е –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ—А–µ–≤—Л—И–∞–µ—В –Є—Е –і–Є–∞–Љ–µ—В—А. –Ь–љ–Њ–≥–Њ—Б–ї–Њ–є–љ—Л–µ –љ–∞–љ–Њ—В—А—Г–±–Ї–Є –Њ—В–ї–Є—З–∞—О—В—Б—П –Њ—В –Њ–і–љ–Њ—Б–ї–Њ–є–љ—Л—Е –±–Њ–ї—М—И–Є–Љ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ–Љ —Д–Њ—А–Љ –Є –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–є. –Ш—Е –њ–Њ–њ–µ—А–µ—З–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Є–Љ–µ–µ—В –і–≤–µ —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–Є (—А–Є—Б. 16). –Ю–і–љ—Г –љ–∞–Ј–≤–∞–ї–Є ¬Ђ—А—Г—Б—Б–Ї–∞—П –Љ–∞—В—А–µ—И–Ї–∞¬ї, —В–∞–Ї –Ї–∞–Ї –Њ–љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Ї–Њ–∞–Ї—Б–Є–∞–ї—М–љ–Њ –≤–ї–Њ–ґ–µ–љ–љ—Л–µ –і—А—Г–≥ –≤ –і—А—Г–≥–∞ –Њ–і–љ–Њ—Б–ї–Њ–є–љ—Л–µ —Ж–Є–ї–Є–љ–і—А–Є—З–µ—Б–Ї–Є–µ –љ–∞–љ–Њ—В—А—Г–±–Ї–Є. –Ф—А—Г–≥–∞—П –љ–∞–њ–Њ–Љ–Є–љ–∞–µ—В —Б–Ї–∞—В–∞–љ–љ—Л–є —А—Г–ї–Њ–љ –Є–ї–Є —Б–≤–Є—В–Њ–Ї. –Ф–ї—П —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А —Б—А–µ–і–љ–µ–µ —А–∞—Б—Б—В–Њ—П–љ–Є–µ –Љ–µ–ґ–і—Г —Б–Њ—Б–µ–і–љ–Є–Љ–Є —Б–ї–Њ—П–Љ–Є, –Ї–∞–Ї –Є –≤ –≥—А–∞—Д–Є—В–µ, —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,335 –љ–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—В–Є –љ–∞–љ–Њ—В—А—Г–±–Ї–Є —Б–∞–Љ–Њ–Њ—А–≥–∞–љ–Є–Ј—Г—О—В—Б—П –≤ —Б–≤—П–Ј–Ї–Є-–ґ–≥—Г—В—Л —Б–µ—З–µ–љ–Є–µ–Љ –±–Њ–ї–µ–µ –Њ–і–љ–Њ–є –і–µ—Б—П—В–Њ–є –Љ–Є–ї–ї–Є–Љ–µ—В—А–∞, —З—В–Њ –і–µ–ї–∞–µ—В –Є—Е –Њ—З–µ–љ—М –Љ–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–Є–Љ–Є –і–ї—П —В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–љ–Њ–≥–Њ–Ї–∞–љ–∞–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–µ—А–µ–і–∞—З–Є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Є–ї–Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–є (—А–Є—Б. 17). –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤—Л—П—Б–љ–Є–ї–Є—Б—М —Б–Њ–≤–µ—А—И–µ–љ–љ–Њ —Д–∞–љ—В–∞—Б—В–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї. –Я–Њ –њ—А–Њ—З–љ–Њ—Б—В–Є –Њ–љ–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ—А–µ–≤–Њ—Б—Е–Њ–і—П—В –ґ–µ–ї–µ–Ј–Њ –Є –±–ї–Є–Ј–Ї–Є –Ї –∞–ї–Љ–∞–Ј—Г, –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ–Њ –Љ–∞—Б—Б–µ —В–∞–Ї–Є–µ —В—А—Г–±–Ї–Є –ї–µ–≥—З–µ –њ–ї–∞—Б—В–Є–Ї–∞. –Ю—Б—В–∞–ї–Њ—Б—М –љ–∞—Г—З–Є—В—М—Б—П –і–µ–ї–∞—В—М –Є—Е –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ –і–ї–Є–љ–љ—Л–Љ–Є вАФ —А–∞–Ј–Љ–µ—А—Л —В—А—Г–±–Њ–Ї —Б–≤—П–Ј–∞–љ—Л —Б –њ—А–Њ—З–љ–Њ—Б—В—М—О –Є–Ј–≥–Њ—В–∞–≤–ї–Є–≤–∞–µ–Љ—Л—Е –≤–µ—Й–µ—Б—В–≤. –Ю–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П, —Г–Ј–Њ—А –Њ–і–љ–Њ—Б–ї–Њ–є–љ–Њ–є –љ–∞–љ–Њ—В—А—Г–±–Ї–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В –µ–µ —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞: –љ–∞–љ–Њ—В—А—Г–±–Ї–Є —Б —А–∞–Ј–љ—Л–Љ–Є —Г–Ј–Њ—А–∞–Љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Љ–µ—В–∞–ї–ї–∞–Љ–Є, –њ–Њ–ї—Г–Љ–µ—В–∞–ї–ї–∞–Љ–Є –Є –њ–Њ–ї—Г–њ—А–Њ–≤–Њ–і–љ–Є–Ї–∞–Љ–Є. –Ю–љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–µ–Ї—А–∞—Б–љ—Л–Љ–Є –њ—А–Њ–≤–Њ–і–љ–Є–Ї–∞–Љ–Є —Н–ї–µ–Ї—В—А–Є—З–µ—Б—В–≤–∞ –Є —В–µ–њ–ї–Њ—В—Л –Є –Љ–Њ–≥—Г—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —В–Њ–љ—З–∞–є—И–Є—Е –Ї–∞–±–µ–ї–µ–є, –њ–Њ–ї—Г–њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤ –Є–ї–Є —Б–≤–µ—А—Е–њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–љ–Є —Б–њ–Њ—Б–Њ–±–љ—Л –Є—Б–њ—Г—Б–Ї–∞—В—М —Н–ї–µ–Ї—В—А–Њ–љ—Л, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —З–µ–≥–Њ –Љ–Њ–≥—Г—В –љ–∞–є—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ —Б–≤–µ—А—Е—В–Њ–љ–Ї–Є—Е –і–Є—Б–њ–ї–µ—П—Е. –Ъ —В–Њ–Љ—Г –ґ–µ –Њ—В–Ї—А—Л–ї–∞—Б—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–Њ–±–Є—А–∞—В—М –Є–Ј –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї —А–∞–Ј–ї–Є—З–љ—Л–µ –љ–∞-–љ–Њ–Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Б –Ј–∞—Ж–µ–њ–∞–Љ–Є –Є —И–µ—Б—В–µ—А–µ–љ–Ї–∞–Љ–Є. –У—А—Г–њ–њ–µ —Г—З–µ–љ—Л—Е –Є–Ј –Р–≤—Б—В—А–∞–ї–Є–є—Б–Ї–Њ–≥–Њ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –Ъ–∞–љ–±–µ—А—А–∞ –љ–∞ –Њ—Б–љ–Њ–≤–µ —Г–≥–ї–µ—А–Њ–і–љ—Л—Е –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї —Г–і–∞–ї–Њ—Б—М —Б–Њ–Ј–і–∞—В—М –µ—Й–µ –Њ–і–љ—Г –љ–Њ–≤—Г—О —Д–Њ—А–Љ—Г —Г–≥–ї–µ—А–Њ–і–∞ вАФ –љ–∞–љ–Њ–њ–µ–љ—Г. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –љ–∞–≥—А–µ–≤–∞ —Г–≥–ї–µ—А–Њ–і–љ–Њ–є –Љ–Є—И–µ–љ–Є –Љ–Њ—Й–љ—Л–Љ –ї–∞–Ј–µ—А–љ—Л–Љ –њ—Г—З–Ї–Њ–Љ —Б –∞–Љ–њ–ї–Є—В—Г–і–Њ–є 10 —В—Л—Б. –Є–Љ–њ—Г–ї—М—Б–Њ–≤ –≤ —Б–µ–Ї—Г–љ–і—Г –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –Њ–Ї–Њ–ї–Њ 1000 ¬∞–° –±—Л–ї –њ–Њ–ї—Г—З–µ–љ –љ–Њ–≤—Л–є –Љ–∞—В–µ—А–Є–∞–ї –≤ –≤–Є–і–µ –Љ–µ–ї—М—З–∞–є—И–µ–є —Б–µ—В–Ї–Є (–њ–µ–љ—Л), —Б–Њ—Б—В–Њ—П—Й–µ–є –Є–Ј –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї. –Я–Њ–ї—Г—З–µ–љ–љ—Л–є –Љ–∞—В–µ—А–Є–∞–ї –Њ–±–ї–∞–і–∞–µ—В –Љ–∞–≥–љ–Є—В–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, —Е–Њ—В—П —Б–∞–Љ —Г–≥–ї–µ—А–Њ–і —В–∞–Ї–Њ–≤—Л—Е —Б–≤–Њ–є—Б—В–≤ –љ–µ –Є–Љ–µ–µ—В. –≠—В–Њ –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–Њ –љ–∞–љ–Њ–њ–µ–љ—Л, –њ–Њ –Љ–љ–µ–љ–Є—О –∞–≤—Б—В—А–∞–ї–Є–є—Б–Ї–Є—Е —Г—З–µ–љ—Л—Е, –љ–∞—А—П–і—Г —Б –Т—Л—Б–Њ–Ї–Њ–є –њ–Њ–≥–ї–Њ—Й–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Ї –Є–љ—Д—А–∞–Ї—А–∞—Б–љ–Њ–Љ—Г –Є–Ј–ї—Г—З–µ–љ–Є—О (–љ–∞–≥—А–µ–≤—Г), –Љ–Њ–ґ–µ—В —Б—Л–≥—А–∞—В—М –≤–∞–ґ–љ–µ–є—И—Г—О —А–Њ–ї—М –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –њ—А–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–Є –Є —Г–љ–Є—З—В–Њ–ґ–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є. –Я—А–Є –≤–≤–µ–і–µ–љ–Є–Є –љ–∞–љ–Њ–њ–µ–љ—Л –≤ –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –њ–Њ—П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –µ–µ –Њ—В—Б–ї–µ–ґ–Є–≤–∞–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –Ј–∞ —Б—З–µ—В –±–Њ–ї–µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –Є–љ—Д—А–∞–Ї—А–∞—Б–љ–Њ–≥–Њ –љ–∞–≥—А–µ–≤–∞ –±–Њ–ї—М–љ—Л—Е —В–Ї–∞–љ–µ–є, –љ–µ —В—А–∞–≤–Љ–Є—А—Г—П —Б–Њ—Б–µ–і–љ–Є–µ –Ј–і–Њ—А–Њ–≤—Л–µ –Ї–ї–µ—В–Ї–Є. –Э–∞–љ–Њ—В—А—Г–±–Ї–Є –Њ–±–ї–∞–і–∞—О—В –Є —А—П–і–Њ–Љ –і—А—Г–≥–Є—Е —Г–љ–Є–Ї–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Є —Б–≤–Њ–є—Б—В–≤, –Ї–Њ—В–Њ—А—Л–µ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е –≥–ї–∞–≤–∞—Е. –Я—А–Є —Н—В–Њ–Љ —Г–≥–ї–µ—А–Њ–і вАФ –љ–µ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –Љ–∞—В–µ—А–Є–∞–ї –і–ї—П –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–Њ–љ –Є –љ–∞–љ–Њ—В—А—Г–±–Њ–Ї. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ–Њ–ї—Г—З–µ–љ—Л –љ–∞–љ–Њ—В—А—Г–±–Ї–Є –Є–Ј –љ–Є—В—А–Є–і–∞ –±–Њ—А–∞, –Ї–∞—А–±–Є–і–Њ–≤ –±–Њ—А–∞ –Є –Ї—А–µ–Љ–љ–Є—П, –Њ–Ї—Б–Є–і–∞ –Ї—А–µ–Љ–љ–Є—П –Є —А—П–і–∞ –і—А—Г–≥–Є—Е –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤. –Т —Б–∞–Љ–Њ–µ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П —Б–Њ–Њ–±—Й–∞–µ—В—Б—П –Њ —Б–Њ–Ј–і–∞–љ–Є–Є –µ—Й–µ –Њ–і–љ–Њ–є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–Є –љ–∞–љ–Њ—Б—В—А—Г–Ї—В—Г—А вАФ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є –љ–∞–љ–Њ—В—А–∞-–≤—Л, –Ї–Њ—В–Њ—А–∞—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–ї–Њ—В–љ—Л–є —Б–ї–Њ–є –љ–∞–љ–Њ–≤–Њ–ї–Њ–Ї–Њ–љ, –њ–µ—А–њ–µ–љ–і–Є–Ї—Г–ї—П—А–љ–Њ –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –њ–Њ–і–ї–Њ–ґ–Ї–Є. –С–ї–∞–≥–Њ–і–∞—А—П –њ–Њ—Б—В–Њ—П–љ–љ–Њ–Љ—Г –Є –±—Г—А–љ–Њ–Љ—Г —А–∞–Ј–≤–Є—В–Є—О –љ–∞–љ–Њ—В–µ—Е–љ–Њ-–ї–Њ–≥–Є–є –±—Г–і–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Њ—Ж–µ—Б—Б –љ–µ–њ—А–µ—А—Л–≤–љ–Њ–≥–Њ –Њ—В–Ї—А—Л—В–Є—П –Є —Б–Њ–Ј–і–∞–љ–Є—П —Б–∞–Љ—Л—Е —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е —Д–Њ—А–Љ –Є —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–µ–є –Њ–±—К–µ–Ї—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –≤—Л—И–µ –≥–µ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –±—Г–і—Г—В –Њ—В–љ–µ—Б–µ–љ—Л –Ї –љ–∞–љ–Њ–Љ–∞—В–µ—А–Є–∞–ї–∞–Љ. |